Cei care cred că pot scăpă uşor de infecţia cu Covid-19, refuzând vaccinul şi alegând să folosească în schimb medicamentele sub formă de pastile, ar trebui să fie îngrijoraţi.
Potrivit specialiştilor, noile ‘tablete-minune’ sunt extrem de toxice şi pot genera aceleaşi efecte adverse ca şi vaccinul anti-covid, dacă nu cumva mult mai severe, scrie BLACKNEWS.RO.
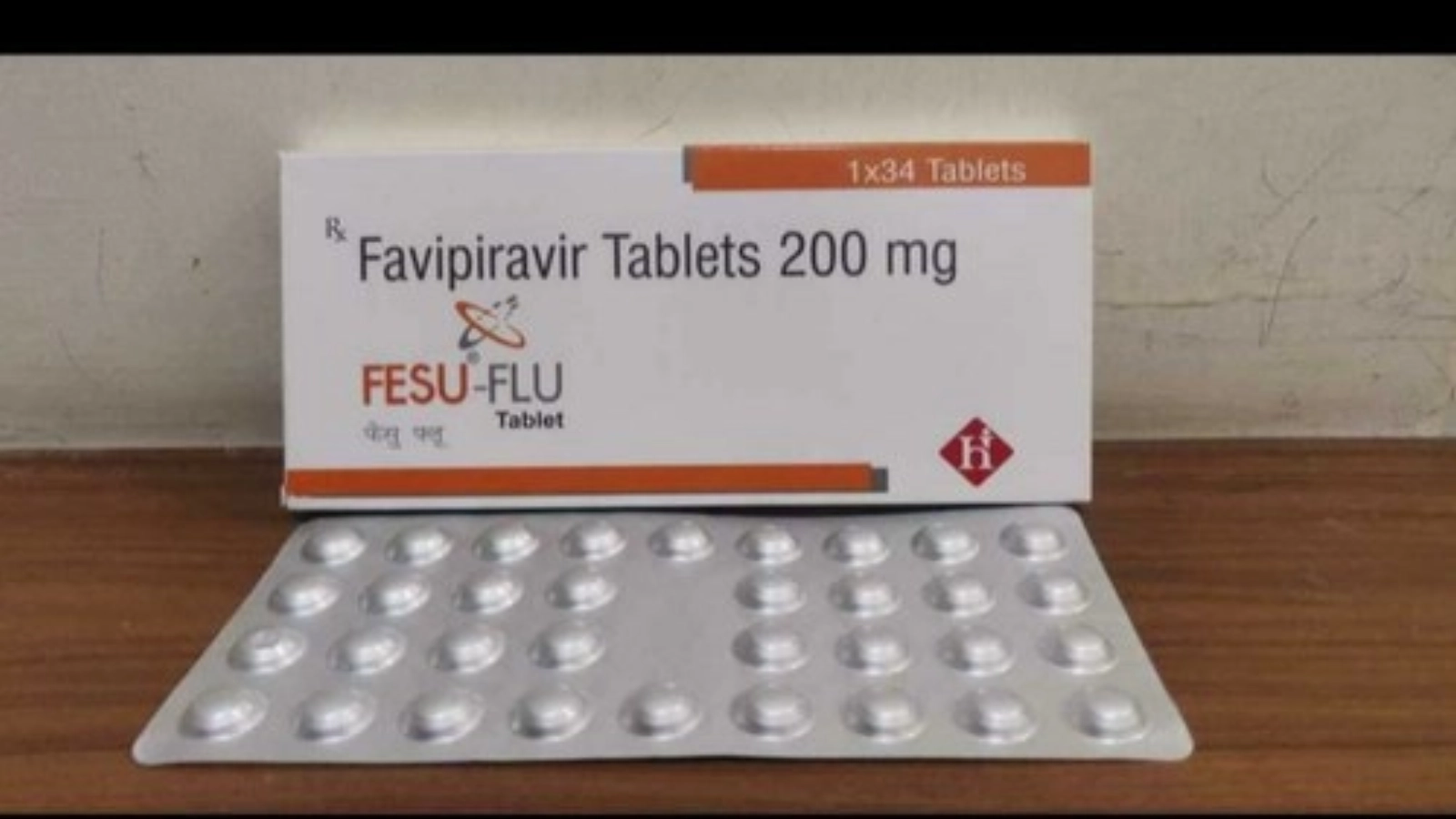
Vă prezentăm mai jos prospectul de folosire în detaliu al medicamentului Favipiravir, aşa cum apare el în SUA, iar concluziile le trageţi singuri.
Favipiravir (Statele Unite ale Americii: nu este disponibil comercial; consultați Restricții de prescriere și acces): informații despre medicamente
Alerte speciale
Actualizări importante COVID-19 ianuarie 2021
În acest moment, deși există o serie de medicamente investigate pentru tratamentul și/sau prevenirea COVID-19, terapia optimă nu a fost stabilită. Continuăm să monitorizăm evoluțiile și să sintetizăm conținutul pe baza experienței clinice ale experților și a literaturii și ghidurilor publicate de la organizațiile majore din domeniul sănătății. Echipele noastre UpToDate și Lexicomp pentru boli infecțioase/îngrijire critică revizuiesc și actualizează continuu conținutul nostru pentru medici în timpul acestei crize.
Mai multe informații pot fi găsite la:
FDA: https://www.fda.gov/emergency-preparedness-and-response/counterterrorism-and-emerging-threats/coronavirus-disease-2019-covid-19
CDC: https://www.cdc.gov/coronavirus/2019-ncov/hcp/therapeutic-options.html
Clinicaltrials.gov: https://clinicaltrials.gov/ct2/results?cond=COVID&term=favipiravir&cntry=&state=&city=&dist=
Categoria farmacologică
Agent antiviral
Dozare: Adult
Notă: Favipiravir este în prezent în investigație pentru utilizare în tratamentul bolii coronavirus 2019 (COVID-19) (vezi ClinicalTrials.gov). În acest moment, datele privind siguranța și eficacitatea sunt limitate. Cu toate acestea, sunt furnizate informații preliminare despre dozare bazate pe dovezile disponibile publicate și pe studiile clinice în curs. Ori de câte ori este posibil, tratamentul trebuie administrat ca parte a unui studiu clinic.
Boala coronavirus 2019 (COVID-19) (utilizare off-label): Oral: Doza și durata optime necunoscute, date limitate disponibile; 1,6 g de două ori pe zi în ziua 1, urmat de 600 mg de două ori pe zi pentru o durată totală de 7 până la 14 zile (Cai 2020; Ivashchenko 2020). Pentru COVID-19 ușor până la moderat, unele piețe internaționale au studiat și aprobat o doză de 1,8 g de două ori pe zi în ziua 1, urmată de 800 mg de două ori pe zi pentru o durată totală de până la 14 zile (FabiFlu 2020; Udwadia 2021).
Dozare: Insuficiență renală: Adult
Insuficiență ușoară până la moderată: Nu sunt recomandate ajustări specifice ale dozelor.
Insuficiență severă: Utilizarea este contraindicată.
Dozare: Insuficiență hepatică: Adult
Insuficiență ușoară până la moderată: Nu sunt recomandate ajustări specifice ale dozelor.
Insuficiență severă: Utilizarea este contraindicată.
Dozare: Adult in varsta
Consultați dozarea pentru adulți.
Forme de dozare: SUA
Informații despre excipienți prezentate atunci când sunt disponibile (limitate, în special pentru medicamente generice); consultați etichetarea produsului specific.
Tabletă, orală:
Generic: 200 mg (agent experimental; nu este disponibil comercial în SUA)
Echivalent generic disponibil: SUA
Da
Restricții de prescriere și acces
Favipiravir nu este disponibil comercial în Statele Unite; cu toate acestea, poate fi disponibil ca parte a unui studiu clinic pentru gestionarea bolii coronavirus 2019 (COVID-19) (a se vedea http://ClinicalTrials.gov).
Utilizare: Off-Label: Adult
Boala coronavirus 2019 (COVID-19)
Probleme de siguranță a medicamentelor
Medicamente de alertă ridicată:
Institutul pentru Practici Sigure de Medicament (ISMP) include acest medicament pe lista sa de medicamente care au un risc crescut de a provoca daune semnificative pacientului atunci cand sunt utilizate in mod gresit.
Reactii adverse
Următoarele reacții adverse și incidente la medicamente sunt derivate din etichetarea produsului, dacă nu se specifică altfel.
Favipiravir este în prezent în investigație pentru utilizare în tratamentul bolii coronavirus 2019 (COVID-19) (a se vedea ClinicalTrials.gov). În acest moment, datele de siguranță sunt limitate.
Frecvența nedefinită:
Cardiovasculare: dureri în piept (Ivashchenko 2020)
Endocrin și metabolic: hiperuricemie (Chen 2020; Sanders 2020)
Gastrointestinale: scăderea apetitului (Cai 2020), diaree (Cai 2020; Ivashchenko 2020; Sanders 2020), greață (Ivashchenko 2020), vărsături (Ivashchenko 2020)
Hematologic și oncologic: scăderea numărului de neutrofile (Sanders 2020)
Hepatic: leziuni hepatice (Cai 2020), creșterea transaminazelor serice (Ivashchenko 2020; Sanders 2020)
Contraindicatii
Hipersensibilitate la favipiravir sau la oricare component al formulării; insuficiență renală sau hepatică severă; sarcina; alaptare.
Avertismente/Precauții
Preocupări legate de efectele adverse:
• Hiperuricemie: Utilizați cu prudență la pacienții cu antecedente de anomalii ale metabolismului acidului uric.
Preocupări legate de boală:
• Guta: A se folosi cu precautie; poate crește acidul uric.
Metabolism/Efecte de transport
Inhibă CYP2C8 (slab)
Interacțiuni medicamentoase
(Pentru informații suplimentare: Lansați programul de interacțiuni medicamentoase)
Vaccin împotriva virusului gripal (viu/atenuat): agenții antivirali (gripa A și B) pot diminua efectul terapeutic al vaccinului împotriva virusului gripal (viu/atenuat). Management: Evitați antiviralele antigripală în perioada care începe cu 48 de ore înainte și se termină la 2 săptămâni după administrarea vaccinului cu virus gripal viu (LAIV). Riscul D: Luați în considerare modificarea terapiei
Pirazinamidă: Favipiravir poate crește efectul advers/toxic al pirazinamidei. Mai exact, riscul de creștere a concentrațiilor de acid uric poate fi crescut. Risc C: Monitorizarea terapiei
Repaglinidă: Inhibitorii CYP2C8 (slăbiți) pot crește concentrația serică a Repaglinidei. Risc C: Monitorizarea terapiei
Considerații de reproducere
Favipiravir este investigat pentru tratamentul bolii coronavirus 2019 (COVID-19) (Cai 2020; Ivashchenko 2020; Udwadia 2021).
Pe baza datelor din studiile de reproducere la animale, utilizarea este contraindicată la pacientele care pot rămâne gravide. Starea sarcinii trebuie evaluată înainte de utilizare. Pacientele care pot rămâne gravide trebuie să utilizeze metode contraceptive eficiente în timpul tratamentului și timp de 1 săptămână după ultima doză de favipiravir. Bărbații cu partenere de sex feminin cu potențial de reproducere ar trebui să utilizeze contracepție eficientă în timpul terapiei și timp de 1 săptămână după ultima doză de favipiravir (Hayden 2019).
Considerații privind sarcina
Favipiravir este în investigație pentru tratamentul bolii coronavirus 2019 (COVID-19); totuși, pacientele gravide nu au fost incluse în studiile clinice inițiale (Cai 2020; Ivashchenko 2020; Udwadia 2021). Pe baza datelor din studiile de reproducere la animale, utilizarea este contraindicată la pacientele gravide (Hayden 2020; Li 2020).
Sunt disponibile informații limitate în urma utilizării la o pacientă tratată pentru COVID-19 imediat postpartum (Jafar 2020).
Riscul de îmbolnăvire severă din cauza infecției cu COVID-19 este crescut la pacientele însărcinate, iar sarcina este una dintre afecțiunile medicale cu risc ridicat definite de CDC. Un risc crescut de rezultate adverse ale sarcinii poate apărea și la pacientele pozitive cu COVID-19 cu infecție simptomatică. Acestea includ nașterea prematură, preeclampsia, coagulopatia și stagnarea sarcinii. Pacienții însărcinate cu infecție simptomatică cu COVID-19 au mai multe șanse să necesite internare la ATI, ventilație mecanică și suport ventilator (ECMO) în comparație cu pacientele simptomatice neînsarcinate. Vârsta mamei și comorbiditățile pot crește, de asemenea, riscul de îmbolnăvire severă la pacientele însărcinate și recent gravide (ACOG 2020; NIH 2021). Informații legate de tratamentul COVID-19 în timpul sarcinii continuă să apară; consultați ghidurile actuale pentru tratamentul pacientelor gravide.
Colegiul American de Obstetricieni și Ginecologi și Societatea pentru Medicină Materno-Fetală au dezvoltat un algoritm pentru a ajuta practicienii să evalueze și să gestioneze pacientele gravide cu COVID-19 suspectat sau confirmat (https://www.acog.org/covid-19; https://www.smfm.org/covid19). Îndrumări intermediare sunt, de asemenea, disponibile de la CDC pentru pacientele gravide care sunt diagnosticate cu COVID-19 (https://www.cdc.gov/coronavirus/2019-ncov/hcp/inpatient-obstetric-healthcare-guidance.html).
Colectarea de date pentru monitorizarea rezultatelor mamei și sugarului în urma expunerii la COVID-19 în timpul sarcinii este în desfășurare. Furnizorii de servicii medicale sunt încurajați să înscrie pacientele expuse la COVID-19 în timpul sarcinii în registrul de sarcină al Organizației Specialiștilor în Informații Teratologice (OTIS) (877-311-8972; https://mothertobaby.org/join-study/).
Considerații privind alăptarea
Nu se știe dacă favipiravir este prezent în laptele matern.
Pe baza datelor din studiile pe animale, alăptarea este contraindicată în timpul tratamentului cu favipiravir (Hayden 2019).
Favipiravir este în studiu pentru tratamentul bolii coronavirus 2019 (COVID-19); cu toate acestea, pacientele care alăptează nu au fost incluse în studiile clinice inițiale (Cai 2020).
Îndrumări intermediare sunt disponibile de la Centrele pentru Controlul și Prevenirea Bolilor pentru îngrijirea pacientelor care alăptează şi care sunt diagnosticati cu COVID-19 (https://www.cdc.gov/coronavirus/2019-ncov/hcp/care-for-breastfeeding- femei.html). Informații legate de COVID-19 și alăptare sunt disponibile și de la Organizația Mondială a Sănătății (https://www.who.int/news/item/28-04-2020-new-faqs-address-healthcare-workers-questions-on -alaptarea-si-covid-19).
Preţ: SUA
Tablete (Favipiravir oral)
200 mg (pe fiecare): 0,01 USD
Exonerare de răspundere: un preț sau un interval de preț reprezentativ AWP este oferit doar ca preț de referință. O gamă este oferită atunci când este disponibil mai mult de un preț AWP al unui producător și utilizează prețul scăzut și ridicat raportat de producători pentru a determina intervalul. Datele de stabilire a prețurilor ar trebui să fie utilizate numai în scopuri de evaluare comparativă și, ca atare, nu ar trebui utilizate singure pentru a stabili sau a adjudeca prețurile pentru funcțiile de rambursare sau de cumpărare sau considerate a fi un preț exact pentru un singur produs și/sau producător. Medi-Span declină în mod expres toate garanțiile de orice fel sau natură, fie că sunt exprese sau implicite, și nu își asumă nicio responsabilitate cu privire la acuratețea prețurilor sau a datelor privind intervalul de prețuri publicate în soluțiile sale. În niciun caz, Medi-Span nu va fi răspunzător pentru daune speciale, indirecte, incidentale sau consecutive rezultate din utilizarea datelor de preț sau interval de preț. Datele de preț sunt actualizate lunar.
Brand Names: International
Avifavir (RU); Avigan (JP); FabiFlu (IN)
REFERINȚE
American College of Obstetricians and Gynecologists (ACOG). COVID-19 FAQs for obstetricians-gynecologists, obstetrics. https://www.acog.org/clinical-information/physician-faqs/covid-19-faqs-for-ob-gyns-obstetrics. Accessed October 22, 2021.
Avigan (favipiravir) [prescribing information]. Tokyo, Japan: Toyama Chemical Co Ltd; January 2014.
Cai Q, Yang M, Liu D, et al. Experimental treatment with favipiravir for COVID-19: an open-label control study. Engineering (Beijing). 2020;6(10):1192-1198. doi:10.1016/j.eng.2020.03.007 [PubMed 32346491]
Chen C, Zhang Y, Huang J, et al. Favipiravir versus arbidol for COVID-19: a randomized clinical trial [published online April 15, 2020]. https://www.medrxiv.org/content/10.1101/2020.03.17.20037432v4. doi:10.1101/2020.03.17.20037432
FabiFlu Glenmark Pharmaceuticals Press Brief. Unlocking the treatment for mild to moderate COVID-19 in India. https://www.glenmarkpharma.com/sites/default/files/Glenmark-FabiFlu-Press-Brief.pdf. Published June 2020. Accessed July 17, 2020.
Furuta Y, Komeno T, Nakamura T. Favipiravir (T-705), a broad spectrum inhibitor of viral RNA polymerase. Proc Jpn Acad Ser B Phys Biol Sci. 2017;93(7):449-463. doi:10.2183/pjab.93.027. [PubMed 28769016]
Hayden FG, Shindo N. Influenza virus polymerase inhibitors in clinical development. Curr Opin Infect Dis. 2019;32(2):176‐186. doi:10.1097/QCO.0000000000000532 [PubMed 30724789]
Ivashchenko AA, Dmitriev KA, Vostokova NV, et al. AVIFAVIR for treatment of patients with moderate COVID-19: interim results of a phase II/III multicenter randomized clinical trial. Clin Infect Dis. Published online August 9, 2020. doi:10.1093/cid/ciaa1176 [PubMed 32770240]
Jafari R, Jonaidi-Jafari N, Dehghanpoor F, Saburi A. Convalescent plasma therapy in a pregnant COVID-19 patient with a dramatic clinical and imaging response: a case report. World J Radiol. 2020;12(7):137-141. doi:10.4329/wjr.v12.i7.137 [PubMed 32850016]
Li L, Wang X, Wang R, Hu Y, Jiang S, Lu X. Antiviral agent therapy optimization in special populations of COVID-19 patients. Drug Des Devel Ther. 2020;14:3001-3013. doi:10.2147/DDDT.S259058 [PubMed 32801640]
National Institutes of Health. COVID-19 Treatment Guidelines Panel. Coronavirus disease 2019 (COVID-19) treatment guidelines. https://www.covid19treatmentguidelines.nih.gov/. Updated October 27, 2021. Accessed October 29, 2021.
Sanders JM, Monogue ML, Jodlowski TZ, Cutrell JB. Pharmacologic treatments for coronavirus disease 2019 (COVID-19): a review [published online April 13, 2020]. JAMA. 2020. doi:10.1001/jama.2020.6019 [PubMed 32282022]
Udwadia ZF, Singh P, Barkate H, et al. Efficacy and safety of favipiravir, an oral RNA-dependent RNA polymerase inhibitor, in mild-to-moderate COVID-19: a randomized, comparative, open-label, multicenter, phase 3 clinical trial. Int J Infect Dis. 2021;103:62-71. doi:10.1016/j.ijid.2020.11.142 [PubMed 33212256]
Topic 127529 Version 33.0






























Comentează